タンパク質を「見る」研究に魅せられて
小祝 孝太郎 研究員
タンパク質は、私たちの体を構成したり、体の中の化学反応を手助けする酵素になったりと、生物が生きていく上で必要不可欠な要素です。タンパク質の分子は、アミノ酸が連なった鎖が組み合わさって、鎖がねじれたり、鎖同士が結びつき合ったりと、とても複雑な構造をとっています。「放射光」と呼ばれる強く明るい光を用いると、タンパク質の構造をまさに「見る」ことができます。今回は、その放射光を用いて、多くの生物に存在する「ノイラミニダーゼ」というタンパク質を見る研究をされている高エネルギー加速器研究機構(KEK)物質構造科学研究所、構造生物学研究センターの小祝孝太郎先生に、タンパク質をどのように「見る」のか、その先には何が見えるのかについてお話を伺ってきました。
放射光でタンパク質を見る
タンパク質の構造解析には、放射光と呼ばれる一種の電磁波が用いられます。普段私たちが目にする可視光や、通信などに利用される赤外線、医療現場などで用いられるX線も電磁波です。一方で、原子を構成している粒子の一つである「電子」を光速に近い速度まで加速し、その動く方向を急に変えると、電子のエネルギーの一部が、まるでその進行方向の変化についていけないかのように、前方へと放出されます。このエネルギーがX線などの電磁波であり、「放射光」と呼ばれています。加速器を構成する電磁石によって、赤外線からX線まで、幅広い波長の放射光を作り出すことが可能で、様々な実験をすることができます。
日本国内にある大型の放射光施設としては、茨城県つくば市のKEKにあるフォトンファクトリー(PF)と、兵庫県佐用郡佐用町にあるSPring-8が運用されています。これらは、シンクロトロンと呼ばれる円形の加速器です。
しかし、原子や分子の瞬間的な動きや、より小さな結晶を用いて分子を観察するには、従来の放射光設備では光の強度が足りないとされていました。そこで考えられたのがX線自由電子レーザー(XFEL)です。加速されて、高エネルギーとなった電子をアンジュレータと呼ばれるたくさんの磁石を並べた構造の中を通すと、電子が周期的にローレンツ力を受けて蛇行することで、放射光が発生します。XFELではこのアンジュレータを直線状に多く配置し、後ろの電子と前の電子から出る光の相互作用によって、位相の揃った強い放射光を作り出すことができます。
このXFELを日本で初めて実装した施設が、SPring-8の隣に作られ、2012年より供用が開始されたSACLAです。小祝先生はSACLAを用いて、「ノイラミニダーゼ」というタンパク質の結晶構造を解析しています。
ノイラミニダーゼと結晶化
ノイラミニダーゼは多くの生物が持っている酵素で、哺乳類では1番と呼ばれるものから4番と呼ばれるものまでの存在が知られています。ヒトの細胞においても、リソソームという細胞小器官にノイラミニダーゼが存在し、糖鎖を切る働きをしています。このノイラミニダーゼの1番が変異を起こすと、精神運動発達遅延や腹部膨満、肝脾腫などの発達障害が起こることがあります。
小祝先生は、こうした発達障害や、ノイラミニダーゼの阻害剤である抗インフルエンザウイルス薬剤の副作用についての研究への応用のために、ノイラミニダーゼの1番について構造決定の研究をしています。
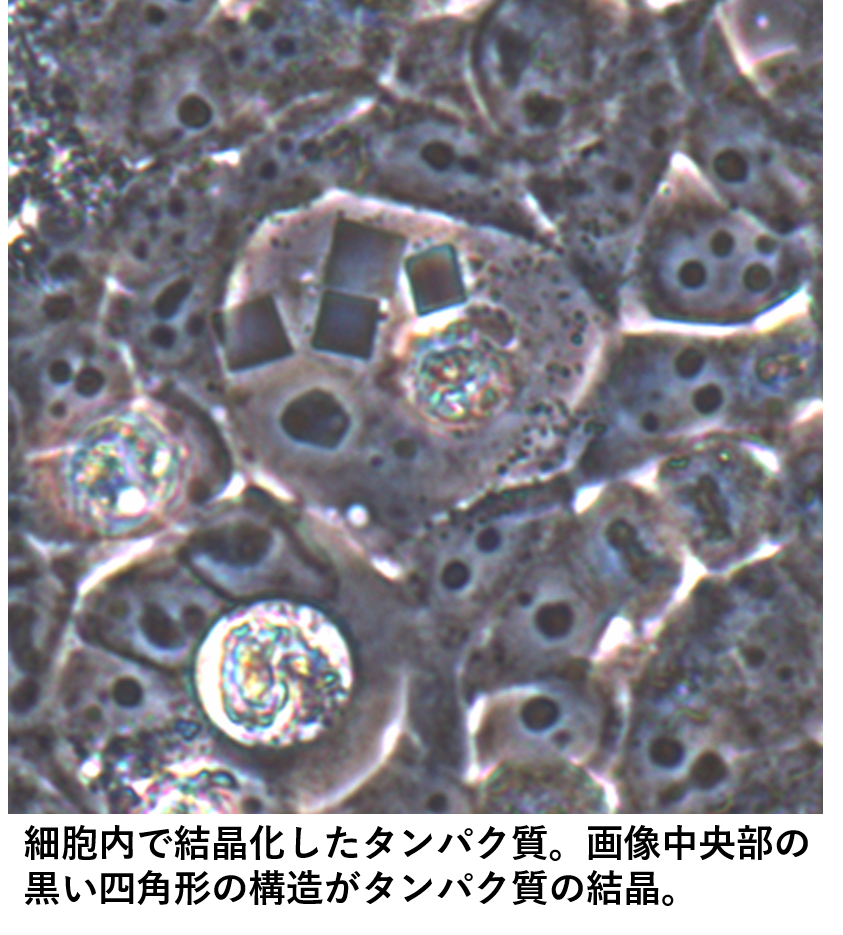
構造の決定は、タンパク質を結晶化するところから始めます。一般的に、結晶は、大腸菌などを用いて解析したいタンパク質を大量に作り出し、そこに様々な試薬を混ぜて作り出します。小祝先生によると、「タンパク質の構造解析の最も大きな難しさはこの過程にある」ということです。どのような試薬を混ぜると結晶化するのかはタンパク質によって異なり、また混ぜてみるまでわからないため、結晶化のためには膨大な試薬の組み合わせを試す必要があります。しかしながら、ごく稀にタンパク質は細胞内でも結晶化することが知られており(図)、細胞内結晶化法と呼ばれています。この細胞内結晶化法では、このような膨大な条件の結晶化は不要で、次世代の結晶化法と考えられています。ノイラミニダーゼの1番では、これまでに、タンパク質を大量に作り出すことができず、結晶化もできていませんでした。しかし、この細胞内結晶化法によって、結晶化することがわかり、結晶構造解析に用いる試みがされています。
このようにして作り出したタンパク質の結晶を、PF、SPring-8、SACLAなどでX線を照射すると、結晶の構造に応じた回析画像が得られます。この画像から、普段目にするリボン状の構造モデルをつくるためには、コンピュータによる解析と同時に、データを読み解く研究者としての経験も必要とされ、ここにも構造解析の難しさがあるということです。
これまでにも、ノイラミニダーゼは結晶化され、それを用いたX線回折画像が得られていましたが、実際に構造を解析するのには不十分なものでした。そのため、小祝先生はすでに発見されていたノイラミニダーゼの細胞内結晶化法を発展させ、よりきれいに大量に抽出する方法を確立させました。この結晶は、サイズは小さくても、大量に抽出できるので、強度が強く波長の短いX線とレーザーの性質を併せ持つSACLAでの解析に向いており、小祝先生は、結晶構造解析に用いられるX線回折画像の撮影に初めて成功したのです。
形に見える生物学に惹かれて
小祝先生がタンパク質の構造解析について研究を始めたのは大学院の博士1年のとき。このテーマを選んだ理由は、「形」だったということです。分子生物学の多くの分野では、電気泳動によって現れるバンドを実験結果の指標としていることが多くあります。しかし、構造解析という分野では、立体構造という「形」が結果として得られます。小祝先生は、構造生物学の魅力は「バンドが出るか出ないかの生物学ではなく、結晶の構造として形に出るのがおもしろい」ところであると言います。また、研究活動について「結果が得られたときの喜びを目指すことがその原動力」であると語り、「細胞内結晶化の他の分野への応用と、新しい放射光施設であるSACLAと結晶構造解析の拠点であるPFのアピールをしていきたいです」と、研究者としての今後の抱負を述べていました。
【取材・構成・文 筑波大学 生物学類1年 曽根原 奎斗】




